近日,我校欧阳松应教授团队在《Nature Communications》上在线发表题为“A bacterial YopJ-family acetyltransferase suppresses host immune response by Nε-acetylation of JAK1”的论文,揭示了嗜肺军团菌效应蛋白Lem17通过双重机制劫持宿主JAK-STAT信号通路、实现免疫逃逸的新机制。
嗜肺军团菌作为一种胞内病原菌,依赖其分泌的300多种效应蛋白劫持宿主功能以促进自身繁殖,其中包括多个YopJ家族乙酰基转移酶。不同于传统的乙酰化转移酶,该家族乙酰基转移酶主要乙酰化修饰宿主免疫信号通路中激酶和连接蛋白的丝氨酸/苏氨酸,抑制宿主的先天免疫防御,促进病原体感染。然而,嗜肺军团菌感染致病过程中,YopJ家族乙酰转移酶如何精准靶向宿主关键信号分子、破坏干扰素应答的分子机制尚不清晰。此前,该团队已在嗜肺军团菌免疫逃逸领域取得系列进展,揭示了效应蛋白LnaB、MavC等在泛素系统调控中的作用,但YopJ家族成员的劫持策略仍有待深入阐明。
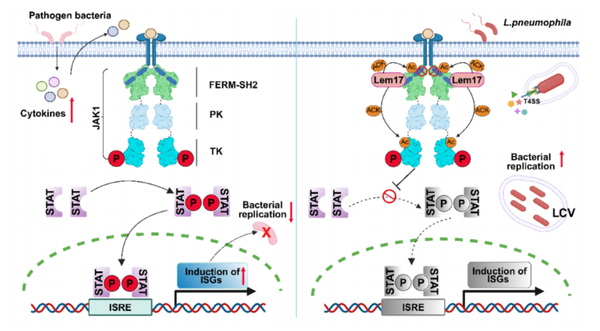
研究团队通过生信分析、细胞生物学、结构解析及生化验证等多种手段,发现与现有YopJ家族乙酰转移酶不同,Lem17是一种靶向目标蛋白赖氨酸残基的YopJ乙酰转移酶。随后通过甲醛免疫沉淀(IP)、质谱及功能验证等手段筛选出Lem17靶向宿主Janus激酶1(JAK1)蛋白。JAK1是JAK-STAT通路的枢纽分子,通过磷酸化下游STAT蛋白,转导干扰素、白介素等多种细胞因子信号,从而调控免疫应答。Lem17能够乙酰化修饰JAK1的多个赖氨酸位点,导致其激酶活性丧失,进而抑制下游STAT信号的转导。同时,研究团队还发现Lem17含有一个保守的、与干扰素、白介素等受体结合JAK1的Box1基序类似的motif,可直接结合JAK1的 FERM结构域,从而阻碍上游受体对JAK1的招募。该研究不仅深化了对病原体免疫逃逸机制的认识,也揭示了乙酰化修饰及JAK-STAT通路在致病菌感染过程中的关键作用。
我校为第一作者单位,生命科学学院陈涛涛副教授、博士研究生郑思如、杨彬彬及卢秋华为本文共同第一作者,欧阳松应教授、苏经迁教授为共同通讯作者。该工作得到国家自然科学基金、省自然科学基金等资助。
原文链接:https://www.nature.com/articles/s41467-026-69623-6
(科学技术处 生命科学学院)
